«HCM ist heute behandelbar»
Therapie und Diagnostik der hypertrophen obstruktiven Kardiomyopathie (HCM) haben in den vergangenen Jahren einen deutlichen Wandel erfahren. Dr. Judith Schwaiger, Hirslanden Klinik im Park, Zürich, berichtete am Zürcher Herz-Kurs, wie präzise Diagnostik und moderne Myosininhibitoren heute viele interventionelle Eingriffe überflüssig machen können.
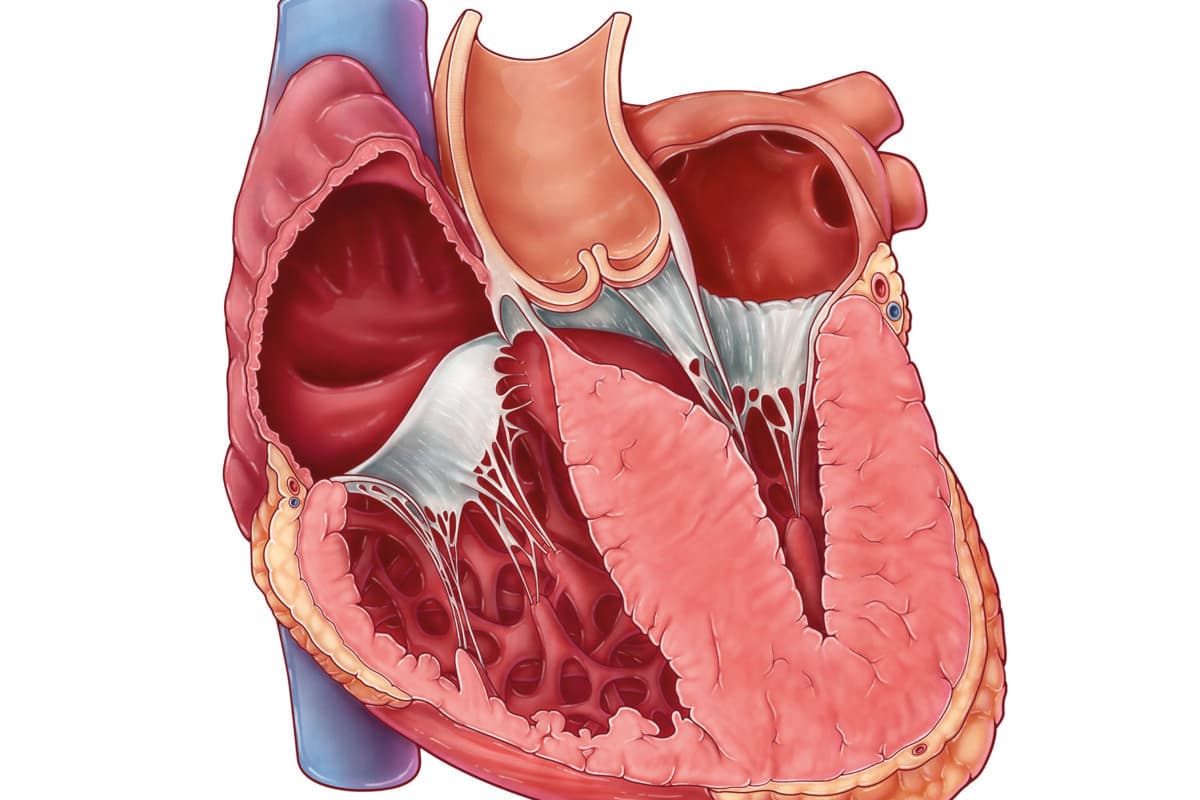
«Die hypertrophe Kardiomyopathie gilt heute als behandelbar», erklärte Dr. Schwaiger. «Bei rund 50 % der Betroffenen verläuft sie prinzipiell benigne.» Entscheidend ist laut der Referentin dabei, zu erkennen, welche Patienten einer besonderen Behandlung bedürfen.
Hyperkontraktilität als Kernproblem
Einer linksventrikulären Hypertrophie können zwar auch einige andere, oft behandelbare, Differenzialdiagnosen zugrunde liegen. Rund 40–60% der Fälle beruhen jedoch auf Mutationen in Genen von Sarkomerproteinen wie MYH7 oder MYBPC3, die zur Dysfunktion des Sarkomers führen können. Bei ihnen spricht man von der klassischen HCM; die Prävalenz liegt bei rund 1:500.
«Während bei Gesunden 40–50 % der aktiven Myosin-Querverbindungen im «Off-State» ruhen, sind es bei HCM-Patienten nur rund 20 %», so Dr. Schwaiger. Das führt zu Hyperkontraktilität, reduzierter Relaxation und ungeordneten Sarkomeren. Die Konsequenzen können kardiale Hypertrophie, mikrovaskuläre Dysfunktion und Fibrosierung sein. Ausserdem kommt es bei rund 70 % der Patienten zu einer Obstruktion des linksventrikulären Ausflusstrakts (LVOTO) und damit zur obstruktiven HCM.
Zusammengenommen verursachen diese Veränderungen die Symptomatik der HCM:
- Brustschmerz, Atemnot
- Palpitationen, Synkopen
- Risiko eines plötzlichen Herztodes
Die Kardiologin räumte aber auch ein, dass nicht alle Patienten gleich schwer betroffen sein müssen: «Selbst innerhalb von Familien kann es sein, dass die Träger einer pathologischen Mutation unterschiedlich stark erkrankt sind.» Einige Patienten sind trotz Vorhandensein einer Mutation gesund.
LVOT-Obstruktion als prognostischer Marker
Gelegentlich liefert ein EKG erste Hinweise auf eine HCM, etwa in Form von High-Voltage-Kriterien oder pathologischen Q-Zacken. Die Diagnose wird jedoch echografisch gestellt, mit Beurteilung der Wanddicke und Abklärung einer eventuellen diastolischen Dysfunktion bzw. einer Obstruktion. Sie gilt als gesichert ab einer nicht anderweitig erklärbaren linksventrikulären Wanddicke ≥ 15 mm, bzw. ab 13 mm bei positiver Familienanamnese oder Genmutation, oder bei apikaler Hypertrophie.
Eine entscheidende Rolle spielt auch das kardiale MRT, das nicht nur einen Überblick über die Anatomie gibt (z. B. zur Darstellung von apikalen Aneurysmen und Differenzialdiagnostik), sondern mittels Bestimmung des Fibrosegrades auch zur Risikostratifizierung beiträgt. «Je höher das LGE-Ausmass, desto höher ist das Risiko für einen sudden cardiac death. Ab einem Fibrosegrad von 15 % des Myokards wird es relevant für die ICD-Indikation», so Dr. Schwaiger.
Eine bestehende LVOTO ist hingegen ein zentraler prognostischer Marker für die Entwicklung einer Herzinsuffizienz. Essenziell ist die Messung der LVOT-Gradienten in Ruhe und nach Provokation (z. B. durch Valsalva-Manöver, schwere Mahlzeit) mittels physikalischer Stressechokardiografie, die in den aktuellen ESC-Leitlinien Klasse-I-Status hat. Dr. Schwaiger betonte, dass die LVOT-Gradienten stark dynamisch, teils tagesabhängig sind. «Viele Patienten mit HOCM werden erst unter physikalischer Belastung obstruktiv durch die erhöhte Herzfrequenz. Wichtig ist bei der physikalischen Stressechokardiografie vor allem auch die Beobachtung in der Erholungsphase, da hier die Gradienten nochmals deutlich ansteigen können. Beinflussende weitere Faktoren sind auch Nahrungsaufnahme oder Alkoholgenuss
Von Betablockern zur molekularen Myosinhemmung
Die klassische Therapie einer HOCM beginnt mit Betablockern (Klasse-I-Empfehlung). Bei Unverträglichkeit oder Unwirksamkeit kommen Verapamil oder Diltiazem infrage. Doch die Wirksamkeit dieser Substanzen ist möglicherweise begrenzt, wie Dr. Schwaiger berichtete: Der Betablocker Metoprolol hat etwa in der Studie MAPLE-HCM die Leistungsfähigkeit der Probanden verschlechtert, und auch relevante Veränderungen bei LVOT-Gradienten, NYHA-Klassifizierung und kardialen Biomarkern blieben aus. «Die Stellung der Betablocker als Erstlinientherapie könnte durch neuere Daten künftig hinterfragt werden.»
Mit dem reversiblen, allosterischen kardialen Myosininhibitor Mavacamten (Klasse-IIa-Empfehlung für die Zweitlinie) steht erstmals eine kausal ansetzende Therapie bei HOCM zur Verfügung, die nicht nur die LVOT-Obstruktion und damit einhergehend die Symptome bessert, sondern potenziell auch die Erkrankungsdynamik verändern soll. «Durch Mavacamten wird der Anteil der aktiven Myosinverbindungen reversibel normalisiert», erklärte Dr. Schwaiger. Damit sinken Hyperkontraktilität und kardiale Biomarker und die diastolische Füllung verbessert sich.
HOCM-Patienten profitierten in der Zulassungsstudie EXPLORER-HCM früh von Mavacamten, mit gesteigerter Leistungsfähigkeit und einer Abnahme der NYHA-Klasse. Auch die LVOT-Gradienten in Ruhe und unter Belastung sanken deutlich. Der Effekt blieb über 3,5 Jahre stabil.
Dr. Schwaiger beschrieb einen Fall aus ihrer Praxis: Ein Patient mit schwerer LVOTO und erhöhtem Risiko für einen SCD zeigte nach zwölf Wochen Therapie mit Mavacamten eine deutliche Verbesserung der Leistungsfähigkeit, LVOT-Obstruktion und auch der diastolischen Parameter. Zudem war sein errechnetes Risiko für einen plötzlichen Herztod innerhalb von fünf Jahren nach zwölf Wochen Behandlung von 9,2 % auf unter 4 % gesunken. «Eine ICD war damit formal nicht mehr indiziert», so die Referentin.
Septale Reduktion bei persistierenden Symptomen
Bei persistierender Symptomatik trotz Medikation kommen interventionelle Verfahren zur Septumreduktion ins Spiel. Die Myektomie stellt den Goldstandard bei jungen und fitten Patienten dar. Im Gegensatz dazu ist die Alkoholablation eher älteren oder komorbiden Patienten vorbehalten, da bei ihr ein etwas höheres Risiko für die Notwendigkeit einer Schrittmacherimplantation besteht.
Dass Mavacamten auch diese Interventionen verhindern kann, zeigt die VALOR-HCM-Studie: Nach 16 Behandlungswochen benötigten viele Patienten keine Septumreduktionstherapie mehr. Indiziert bleibt die Septumreduktion insbesondere bei Patienten, die ohnehin wegen einer anderen Klappenerkrankung operiert werden müssen, sowie bei Frauen mit Kinderwunsch, bei denen Mavacamten nicht infrage kommt.
Vorhofflimmern bei HCM: Konsequente Therapie erforderlich
HCM-Patienten mit Vorhofflimmern sind oft stark symptomatisch und haben ein hohes Schlaganfallrisiko. Hier ist laut Dr. Schwaiger eine konsequente Strategie angezeigt. «Sie sollten unabhängig vom CHA₂DS₂-VASc-Score antikoaguliert werden.»
Zur Rhythmuskontrolle stehen Amiodaron oder Disopyramid zur Verfügung, ergänzt durch die Radiofrequenz-Ablation. Deren Erfolgsrate liegt bei rund 60%, also geringfügig niedriger als bei Patienten ohne HCM.
Zürcher Herzkurs, 6. November 2025, Zürich
