Ceralasertib: Erste Erfolge mit ATR-Inhibition
Ein Drittel der klarzelligen Karzinome weist einen ARID1A-Defekt auf. Ceralasertib wirkt gegen diese Alteration selektiv toxisch, weshalb der Inhibitor in der Studie ATARI abhängig vom Mutationstatus alleine oder in Kombination mit PARP-Inhibitoren geprüft wurde.
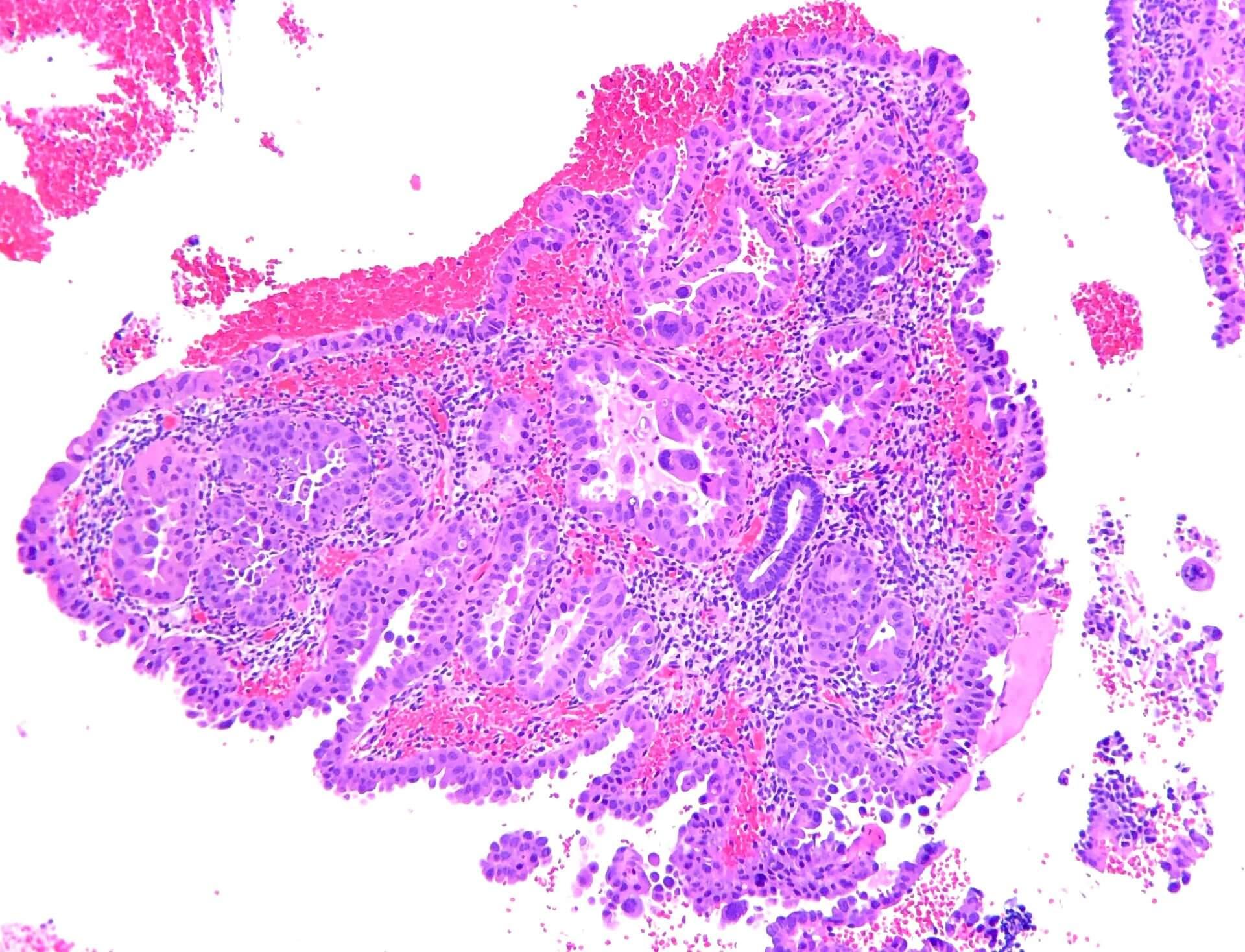
Klarzellige Karzinome und andere ungewöhnliche gynäkologische Tumore haben noch immer eine schlechte Prognose, erinnert Dr. Susana Banerjee, Institute of Cancer Research, London (1). Präklinische Untersuchungen hätten belegt, dass ATR-Inhibitoren selektiv Zellen mit ARID1A-Defekten abtöten können. Diese treten bei 30–40 Prozent der klarzelligen und endometroiden Karzinome auf. Ausserdem steigere die ATR-Hemmung die Zytotoxizität von PARP-Inhibitoren.
Die Referentin präsentierte nun die ersten Ergebnisse der ENGOT/GYN1/NCRI-ATARI-Studie für die jeweils ersten 29 Patientinnen aus allen drei Kohorten: die Forscher wendeten dabei den ATR-Inhibitor Ceralasertib gegen seltene gynäkologische Tumoren an. Teilnehmerinnen mit einem klarzelligen Karzinom und Verlust der ARID1A-Aktivität nahmen die Substanz als Monotherapie ein. Bei erhaltener Proteinfunktion kam ergänzend Olaparib zum Einsatz.
Zusätzlich behandelten die Forscher die Kohorte, die Erkrankte mit gynäkologischen Malignomen anderer Histologien umfasste, unabhängig vom ARID1A-Status mit der Kombinationstherapie.
Medianes Ansprechen von 24 Wochen in Kohorte eins
Vier Frauen (14%) entwickelten unter alleinigem Ceralasertib eine bestätigte partielle Remission, insgesamt lag das PFS nach 16 Wochen bei 45 Prozent (95 %-KI: 27–62). Das Ansprechen hielt median 24 Wochen an. In der zweiten Kohorte erzielte die Kombination ähnliche Ansprechraten, allerdings wirkte diese im Median nur acht Wochen.
Der Arm mit nicht-klarzelligen Tumoren erreichte eine bestätigte OR bei sechs Erkrankten und damit als einziger das Studienziel. Das PFS nach 16 Wochen betrug 54 Prozent (95 %-KI: 35–70) und die mediane Ansprechdauer 41 Wochen.
Primärer Endpunkt unter Monotherapie verfehlt
Dr. Banerjee schätzte die Toxizität von Ceralasertib als beherrschbar ein. Nur 6 Prozent aller Behandelten brachen die Therapie wegen Nebenwirkungen ab. Abschliessend betonte die Referentin, der Wirkstoff habe allein und in Kombination mit Olaparib Zeichen klinischer Aktivität bei diesen seltenen Krebserkrankungen demonstriert.
Prof. Dr. Jean-Emmanuel Kurtz, Universitätsklinikum Strassburg, diskutierte die Ergebnisse kritischer (2). Die Ceralasertib-Monotherapie habe nicht ausgereicht, den angestrebten primären Endpunkt zu erreichen. «Einzelne Patientinnen profitierten jedoch vom Medikament. 31 Prozent wurden länger als sechs Monate behandelt», räumte der Diskutant ein.
Bei der Kombinationstherapie bleibt der HRD/BRCA-Status und das platinfreie Intervall unklar. Der Experte bezweifelt, dass PARP-Inhibitoren einen zusätzlichen Nutzen in ARID1A-kompetenten Zellen mit intakter DNA-Reparatur bringen. In der gemischten Kohorte hätten sich alle Patientinnen mit ARID1A-Defekt als Non-Responder erwiesen. Ergebnisse anderer Studien deuten darauf hin, dass dieser Zustand eine Resistenz gegen PARP-Inhibitoren vermittelt.
«Ich denke, man hat eine gewisse Wirksamkeit beobachtet, wobei man über das Ausmass diskutieren kann», schloss Prof. Kurtz. Allgemein benötige es neuer Behandlungsoptionen bei klarzelligen Karzinomen.
Referenzen
- Banerjee S, et al. ATR inhibitor alone (ceralasertib) or in combination with olaparib in gynaecological cancers with ARID1A loss or no loss - results from the ENGOT/GYN1/NCRI ATARI trial. ESMO Gynaecological Cancers Congress 2023, Abstract 34O
- Kurtz JE. ESMO Gynaecological Cancers Congress 2023; Diskussion zu Vortrag 34O, ESMO Gynaecological Cancers Congress 2023